- Qu'est-ce qu'un pH-mètre mesure réellement en sortie d'électrode ?
- De quoi se compose une sonde pH ?
- Comment marchent les différents types de pH-mètres ?
- Pourquoi le pH-mètre fonctionne-t-il comme un voltmètre à haute impédance ?
- Comment l'équation de Nernst relie le signal en mV au pH affiché ?
- Que compense la température sur un pH-mètre et quelles sont ses limites ?
- Comment étalonner un pH-mètre ?
- Qu'est-ce qu'un pH-mètre mesure réellement en sortie d'électrode ?
- De quoi se compose une sonde pH ?
- Comment marchent les différents types de pH-mètres ?
- Pourquoi le pH-mètre fonctionne-t-il comme un voltmètre à haute impédance ?
- Comment l'équation de Nernst relie le signal en mV au pH affiché ?
- Que compense la température sur un pH-mètre et quelles sont ses limites ?
- Comment étalonner un pH-mètre ?
- Un pH-mètre mesure une différence de potentiel en millivolts entre une électrode de verre et une électrode de référence, puis la convertit en pH.
- La conversion suit l'équation de Nernst : à 25 °C, chaque unité de pH correspond à 59,16 mV. Une variation de 0,01 pH représente environ 0,6 mV.
- La compensation de température corrige la pente de Nernst liée à l'instrument, mais elle ne modifie pas la valeur réelle du pH de la solution, qui change chimiquement avec la température.
- Le pH de l'eau pure en est la meilleure illustration : il vaut 7,47 à 0 °C, 7,00 à 25 °C et 6,63 à 50 °C.
- L'électrode de verre présente une résistance de 10⁸ Ω. Le pH-mètre doit donc disposer d'une impédance d'entrée supérieure à 10¹² Ω et travailler avec un courant de l'ordre de 10⁻¹² A.
- Un étalonnage en 2 ou 3 points avec des tampons frais reste la seule façon de lier correctement la tension mesurée au pH affiché.
- La membrane de verre doit rester hydratée en permanence : un stockage à sec impose une réhydratation d'au moins 24 heures avant toute mesure fiable.
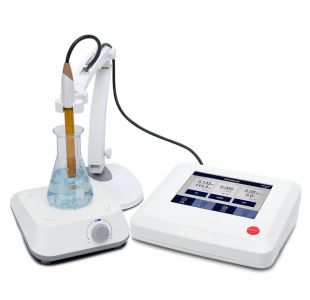
Le fonctionnement d’un pH-mètre repose sur la mesure d’une tension électrique générée par une électrode plongée dans une solution. L’appareil ne mesure pas directement les ions hydrogène, mais un signal électrique exprimé en millivolts. Cette tension est ensuite convertie en valeur de pH à l’aide d’une relation électrochimique issue de l’équation de Nernst. Le dispositif associe une électrode de mesure, une électrode de référence et un système électronique capable d’interpréter des variations de potentiel très faibles. La précision de la mesure dépend de paramètres tels que la température, l’état de l’électrode et les conditions de mesure.
Qu'est-ce qu'un pH-mètre mesure réellement en sortie d'électrode ?
De quoi se compose une sonde pH ?
Électrode de mesure : ampoule en verre
- L'hydratation de la membrane : un verre sec répond mal ou pas du tout ; une réhydratation d'au moins 24 heures est requise après stockage à sec.
- Le vieillissement : avec l'usage, la couche de gel hydratée s'altère et la résistance de la membrane augmente progressivement.
- La température : elle modifie à la fois la mobilité ionique et la résistance de la membrane, ce qui affecte la vitesse de réponse et la valeur de la pente.
Électrode de référence : potentiel stable
Électrode combinée et capteur de température intégré
- La température est mesurée au plus près de la membrane, là où la réaction physico-chimique a lieu.
- La compensation de pente est automatique et fiable, sans décalage lié à un capteur distant.
- Le temps de stabilisation après changement de milieu est réduit, car les trois grandeurs (pH, température, potentiel de référence) s'équilibrent ensemble.
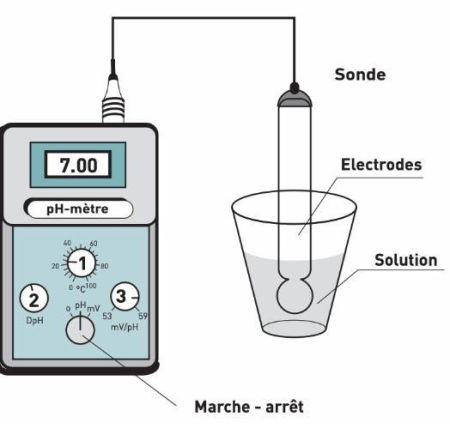
Comment marchent les différents types de pH-mètres ?
Fonctionnement du pH-mètre portable
Le pH-mètre portable est conçu pour des mesures réalisées directement sur site. Il fonctionne avec une électrode intégrée ou interchangeable reliée à un boîtier compact. L’utilisateur immerge l’électrode dans la solution. Le capteur détecte l’activité des ions hydrogène et génère une tension. Le circuit interne convertit cette tension en valeur de pH affichée à l’écran. Ce type d’appareil fonctionne sur batterie. Il permet des mesures ponctuelles dans des environnements extérieurs, comme le contrôle de l’eau ou du sol.
Fonctionnement du pH-mètre de laboratoire
Le pH-mètre de laboratoire est utilisé dans un environnement contrôlé. Il fonctionne avec une électrode séparée reliée à une unité de mesure fixe. L’électrode est plongée dans l’échantillon. Le système capte la différence de potentiel entre l’électrode de mesure et l’électrode de référence. Cette différence est amplifiée puis convertie en valeur de pH. Ce type d’appareil intègre des fonctions de calibration, de compensation de température et de stabilisation du signal. Il permet d’effectuer des analyses répétées avec un suivi des paramètres de mesure.
Fonctionnement du pH-mètre en ligne
Le pH-mètre en ligne est intégré dans un processus industriel. Il fonctionne en continu, sans intervention manuelle. L’électrode est installée directement dans une canalisation ou une cuve. Elle mesure en permanence l’activité des ions hydrogène dans le flux de liquide. Le signal est transmis à un système de contrôle. Ce système convertit la tension en valeur de pH et peut déclencher des actions automatiques, comme l’ajustement d’un dosage chimique.
Ce fonctionnement permet un suivi continu du pH dans des applications comme le traitement des eaux ou les procédés industriels.
Pourquoi le pH-mètre fonctionne-t-il comme un voltmètre à haute impédance ?
Paramètres électriques influençant la mesure du pH
- Résistance de l'électrode de verre : environ 10⁸ Ω (100 mégaohms).
- Impédance d'entrée requise du pH-mètre : supérieure à 10¹² Ω.
- Courant de mesure : de l'ordre de 10⁻¹² A.
- Sensibilité : 59,16 mV par unité de pH à 25 °C, soit environ 0,6 mV pour 0,01 pH.
- Incertitude instrumentale sur la tension : typiquement 0,1 mV, ce qui représente moins de 0,002 unité de pH négligeable face aux autres sources d'erreur.
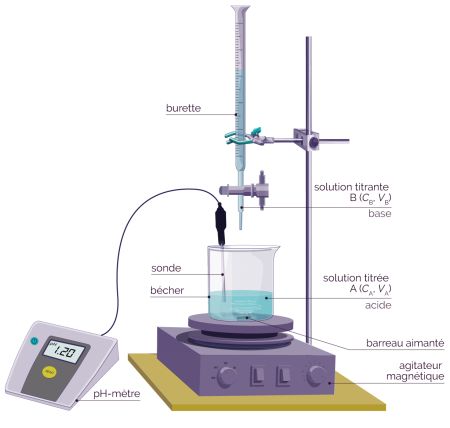
Comment l'équation de Nernst relie le signal en mV au pH affiché ?
Définition de la pente électrochimique
Variation de la pente en fonction de la température
| Température | Pente théorique |
|---|---|
| 0 °C | 54,20 mV/pH |
| 20 °C | 58,16 mV/pH |
| 25 °C | 59,16 mV/pH |
| 37 °C | 61,54 mV/pH |
| 50 °C | 64,12 mV/pH |
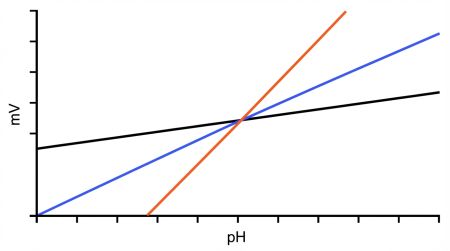
Que compense la température sur un pH-mètre et quelles sont ses limites ?
Correction de la pente de Nernst par la compensation
Mythe : la compensation de température « ramène » le pH mesuré à sa valeur à 25 °C.
Réalité : le pH-mètre affiche le pH réel à la température de mesure, corrigé uniquement pour les effets instrumentaux liés à la pente. Le pH de l'échantillon à 50 °C est intrinsèquement différent de son pH à 25 °C.
Variation du pH de l’eau avec la température
- À 0 °C, le pH de l'eau pure est de 7,47 — l'eau est neutre, mais son pH n'est pas 7.
- À 25 °C, le pH de l'eau pure est de 7,00 — c'est la valeur de référence.
- À 50 °C, le pH de l'eau pure est de 6,63 — l'eau reste neutre, mais son pH a chuté.
Bonnes pratiques thermiques sur le terrain pour des mesures stables
- Étalonner et mesurer à la même température : une électrode calibrée à 20 °C utilisée à 35 °C introduit une erreur systématique difficile à corriger.
- Placer le capteur de température au plus près de la membrane afin d'éviter tout décalage entre la température mesurée et celle à laquelle la réaction électrochimique se produit.
- Attendre l'équilibre thermique avant de lire : plonger une électrode froide dans un échantillon chaud génère une instabilité temporaire pouvant durer plusieurs minutes.
- Mesurer l'échantillon à sa température réelle plutôt que de le ramener à 25 °C, ce qui modifierait ses équilibres chimiques.
- En environnement froid (en dessous de 10 °C), prévoir un temps de stabilisation plus long car la résistance de la membrane augmente fortement à basse température.
Comment étalonner un pH-mètre ?
Étalonnage en 2 points ou en 3 points
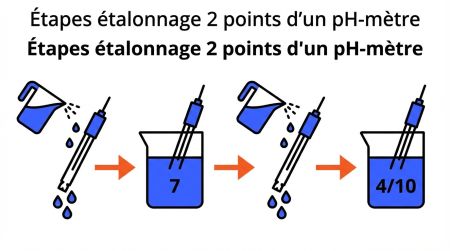
Un étalonnage en 2 points couvre la majorité des besoins de mesure. La procédure se déroule en plusieurs étapes :
- L’électrode est rincée à l’eau déminéralisée afin d’éliminer les résidus.
- Elle est ensuite plongée dans une solution tampon pH 7. La stabilisation du signal est attendue avant validation.
- L’électrode est de nouveau rincée, puis immergée dans un second tampon (pH 4 ou pH 10) selon la plage de mesure.
- Une fois la stabilisation atteinte, le second point est validé.
L’utilisation de solutions tampon fraîches est requise pour garantir la cohérence de l’étalonnage. Un étalonnage en 3 points est utilisé lorsque la plage de mesure est étendue ou lorsque la précision attendue est plus stricte. Un troisième tampon permet d’améliorer l’ajustement sur l’ensemble de la plage.
Vérification de la pente et du point zéro
Après l’étalonnage du pH-mètre, l’appareil affiche des paramètres permettant de vérifier la cohérence de la calibration. La pente doit être comprise entre 95 % et 103 % de la valeur théorique. Le point zéro doit se situer autour de pH 7. Le potentiel d’offset doit rester dans une plage de ±15 mV. Une valeur en dehors de ces plages indique une dérive de l’électrode ou une contamination.
Contrôle de la mesure après étalonnage
Un contrôle complémentaire permet de valider la précision de la mesure. L’électrode est plongée dans une solution tampon de référence dont la valeur est connue et différente de celles utilisées pour l’étalonnage. La valeur affichée est ensuite comparée à la valeur théorique. Un écart significatif indique une anomalie liée à l’électrode ou à la procédure d’étalonnage.
Nos ph-mètres les plus populaires sur hellopro.fr



 Sdl100
Sdl100